Obwohl Knicklichter allseits bekannt sind, ist ihre Funktionsweise den meisten Menschen nicht bewusst.
Geräte und Chemikalien:
Knicklichter, UV-Lampe.
Versuchsdurchführung:
In einem abgedunkelten Raum werden ungeknickte Knicklichter mit UV-Licht beleuchtet. Anschließend wird ein Knicklicht ohne UV-Bestrahlung an einer einzelnen Stelle geknickt.
Beobachtung:
Auch ohne die Knicklichter zu knicken fluoreszieren sie unter UV-Beleuchtung in verschiedenen Farben. Dabei ist die Fluoreszenz nicht im gesamten Knicklicht zu beobachten, sondern auf ein zweites Röhrchen beschränkt, dass im Inneren des Knicklichts liegt (siehe Abbildung A). Beim Knicken bricht das innere Röhrchen sicht- und hörbar und an der Bruchstelle ist Fluoreszenzlicht wahrzunehmen, das sich langsam im Knicklicht verteilt.
Deutung:
Knicklichter bestehen aus einem biegsamen Kunststoffröhrchen mit einem darin eingelassenen Glasröhrchen (siehe Abbildung B), die eine Wasserstoffperoxidlösung räumlich von einer Oxalsäureesterlösung (z. B. Bis(2,4,6-trichlorphenyl)oxalat) trennen. Zudem enthält eines der Röhrchen einen Fluoreszenzfarbstoff, der je nach gewünschter Leuchtfarbe des Knicklichts variiert.

Abbildung: (A) Verschiedenfarbige Knicklichter im ungeknickten Zustand unter UV-Licht. (B) Schematische Darstellung der Funktion von Knicklichtern.
Beim Knicken des Knicklichts bricht das Glas und die beiden Flüssigkeiten mischen sich. Das Wasserstoffperoxid reagiert mit dem Oxalsäureester zu 1,2-Dioxetandion, das hochreaktiv ist und zu zwei Kohlenstoffdioxidmolekülen zerfällt (siehe Abbildung 66). Dabei liegt eines der Moleküle in einem angeregten Singulettzustand vor, dass seine Energie auf die in der Mischung vorhandenen Fluoreszenzfarbstoffe übertragen kann. Bei der Abregung der Farbstoffmoleküle wird diese Energie wiederum in Form von Photonen abgegeben, so dass ein Leuchten zu beobachten ist. Der Fluoreszenzfarbstoff liegt nach der Reaktion unverändert vor, so dass er, auch nachdem das Knicklicht nicht mehr leuchtet, von UV-Licht zur Fluoreszenz angeregt werden kann.
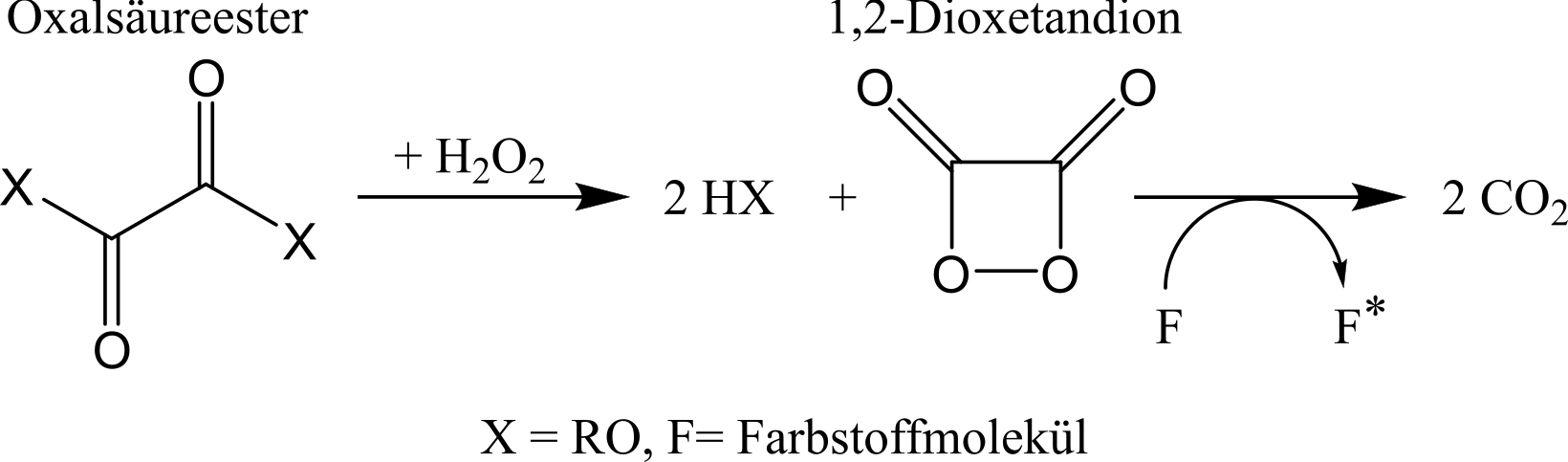
Abbildung: Allgemeiner Reaktionsmechanismus für die Reaktion eines Oxalsäureesters mit Wasserstoffperoxid in einem Knicklicht.
Anmerkungen zur Deutung des Experiments:
In den bisherigen Experimenten erfolgte eine Anregung von Fluoreszenzfarbstoffen immer mithilfe von energiereichem Licht. Es bestehen jedoch weitere Möglichkeiten, dem System die benötigte Energie zuzuführen. Wird ein Molekül infolge einer chemischen Reaktion zur Emission eines Photons angeregt, so spricht man von Chemolumineszenz. Dabei gibt entweder eines der Reaktionsprodukte, das sich in einem angeregten Zustand befindet, die Energie selbst unter Emission eines Photons ab, oder überträgt sie – wie in diesem Fall – auf einen an der Reaktion unbeteiligten Fluoreszenzfarbstoff (Wöhrle & Tausch, 1998).
Die Behandlung der Chemilumineszenz bietet sich in vielerlei Hinsicht an. Zum einen kann das Phänomen der Fluoreszenz noch einmal an einem für die SuS bekannten Alltagsgegenstand betrachtet werden. Zudem kann in diesem Zuge auch auf die Relevanz der Chemielumineszenz für biolumineszente Prozesse in der Natur, z. B. bei Tieren und Einzellern, verwiesen werden. Die Verwendung von Knicklichtern bietet sich zusätzlich auch zur Ausbildung eines situationalen Interesses an. Zudem ist die strahlungslose Energieübertragung von einem Molekül auf ein anderes auch von elementarer Bedeutung für einige der nachfolgenden Experimente.
Literatur:
- Salter, C., Range, K., & Salter, G. (1999). Laser-Induced Fluorescence of Lightsticks. Journal of Chemical Education, 76(1), 84. DOI: 10.1021/ed076p84.
- Wöhrle, D., Tausch, M. W., & Stohrer, W.‑D. (1998). Photochemie: Konzepte, Methoden, Experimente (1st ed.). Weinheim: Wiley-VCH.
- von Hoff, E. (2020). Entwicklung und Evaluation von Konzepten und Formaten zum Wissenstransfer von der Forschung in die Schule und Öffentlichkeit - Am Beispiel des SFB 803 (Dissertation). Georg-August-Universität Göttingen, Göttingen. Abrufbar unter http://hdl.handle.net/21.11130/00-1735-0000-0005-14C7-4.

